亨廷顿病临床试验公告:亨廷顿蛋白降低药物将于2015年进入I期试验
一项针对亨廷顿病的令人振奋的治疗方案临床试验计划于2015年开展。第一步是确保其安全性。

一项于 2015 年宣布的全新临床试验旨在测试一种“降低亨廷顿蛋白”的疗法,称为反义寡核苷酸 (ASO),该疗法直接攻击突变亨廷顿蛋白。我们对此感到非常兴奋——这是有史以来首次针对人类 HD 的试验,旨在从根本上解决 HD 问题,并且在动物模型中显示出巨大的希望。有什么内幕消息吗?
一种针对亨廷顿病基因的潜在药物
这项已公布的临床试验代表了加利福尼亚州的Isis制药公司与瑞士制药巨头罗氏的合作。这种名为ASO-HTT-Rx的药物是一种通过靶向基因本身来治疗亨廷顿病的疗法。
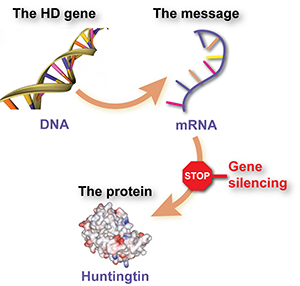
亨廷顿病问题的核心在于有缺陷的DNA序列——亨廷顿基因中CAG构建模块的异常延长。突变基因中包含的指令首先被复制成中间的’信使’拷贝,然后从中产生有害蛋白质。因此,突变基因是问题的根源,但它之所以有害,是因为细胞利用基因中的信息制造有害蛋白质。
ASO-HTT-Rx 背后的策略是“射杀信使”,通过破坏信使副本来攻击基因和蛋白质之间的中间步骤。
这些类型的药物被称为“反义寡核苷酸”,或 ASO。它们是一种合成的 DNA 样分子,可以进入细胞,粘附到突变亨廷顿 RNA 信息上,并导致其降解。如果它像预测的那样发挥作用,那么这种疗法将阻止亨廷顿蛋白的产生——一种“降低亨廷顿蛋白”的策略,从长远来看,它有可能减缓或阻止疾病的进展。
每个ASO都有一个可以调整的基本结构,帮助它粘附在正确的目标信息上,同时忽略细胞中数千个其他信息。这有点像您去五金店配钥匙时——店员选择匹配的空白钥匙,然后刻上正确的凹槽序列以适合您的锁,而不适合您邻居的锁。对于ASOs来说,Isis的科学家们使用他们既定的’骨架’分子并对其进行定制,使药物只攻击亨廷顿信息。
这一切听起来像是尖端技术,但好消息是Isis此前已经在人类大脑中测试过基于ASO的药物,用于治疗ALS(卢伽雷氏病或运动神经元病)和SMA(脊髓性肌萎缩症),且没有报告任何安全性问题。
药物递送
ASOs与传统药物治疗的一个主要区别是,它们不能以口服药片的形式服用,而必须直接递送到神经系统。
为了进入大脑,ASO-HTT-Rx将通过插入脊髓下部脑脊液空间的针头给药。如果这听起来很极端,请放心,这种方法在医学多个领域都是常规使用的。癌症医生使用类似的策略向脑瘤患者输送化疗药物。更常见的是,许多女性在分娩时接受类似的’硬膜外’止痛药物输送。
像ASO-HTT-Rx这样的药物的一个主要优势是,研究人员认为可以间歇性给药仍能保持效果。科学家们将这种针对亨廷顿病的间歇性治疗方法称为’亨廷顿假期’;旨在让大脑从突变型亨廷顿蛋白造成的损害中得到恢复性休息。
一旦注入脑脊液中,ASO-HTT-Rx需要约4至6周才能发挥作用,根据动物研究,我们认为沉默效果将持续约4个月。目前,研究设计要求患者每月接受一次药物治疗。
“与 ASO-Htt-Rx 类似的药物已安全地恢复了 HD 动物模型中的健康行为,将治疗方法转移到人类身上对于整个 HD 社区来说是一个令人兴奋的步骤。尽管这项科学令人兴奋,但第一个计划的试验严格旨在了解该药物是否安全。”
安全第一
决定在2015年推进临床试验是学术界和工业界众多研究人员超过十年工作的成果。经ASO-Htt-Rx治疗的亨廷顿病实验室小鼠显示出显著益处——即使在它们出现症状后进行ASOs治疗也能改善其大脑和行为。
Isis研究人员和伦敦大学学院的Sarah Tabrizi教授(ASO-HTT-Rx研究的全球负责人)强调,这第一个临床试验纯粹是为了评估其安全性。
这是一个关键点。尽管这项科学如此令人振奋,但第一个计划中的试验严格设计用于了解药物是否安全。直接向神经系统注射任何药物都不能掉以轻心——所有潜在风险和副作用都必须在少数志愿患者身上进行详尽检查。
临床试验剖析
所有I期临床试验首要目标都是评估新药的安全性和耐受性。这意味着一小组患者(可能约36人)将接受不同剂量的ASO-Htt-Rx治疗,以确定药物是否有不良副作用,并帮助找到最佳剂量。
约25%的参与患者将接受安慰剂注射(不含任何药物)作为对照组。医生将监测患者对治疗的症状反应,但本试验的主要重点是关于这种新药是否安全。
一旦药物在I期被认定为安全,就可以进入II期。在第二步中,医生可以招募更多患者,开始研究药物在治疗疾病症状方面的有效性。在第一次试验确定安全性和剂量后,研究人员现在可以提出问题,’这种治疗是否能改善人们的亨廷顿病症状(或使其恶化!)’?
如果II期试验结果积极,III期试验将涉及更多患者,仔细检查药物的副作用、有效性和安全性。成功的III期试验是制药公司获得国家监管机构药物批准所需的结果类型。
图片来源:Shutterstock
这对亨廷顿病患者意味着什么?
即使一切进展顺利,将药物推向市场的整个过程也需要数年时间。如果ASO-Htt-Rx在刚刚宣布的I期研究中被证明是安全的,这第一个结果只是临床试验漫长道路的开始。这条路上的每个试验,I期、II期和III期,都将涉及相对较少的治疗患者。此外,在每个试验中,一些志愿者将接受安慰剂治疗,作为接受HTT-ASO-Rx患者的对照组。
HTT-ASO-Rx的I期试验患者将仅从欧洲和加拿大的几个医疗中心招募。一小部分指定的亨廷顿病研究中心将在2015年初宣布,并寻求招募试验参与者。招募对象将是处于亨廷顿病早期阶段的人,但具体入组标准、地点和时间尚未公开。我们确切知道,幕后正在进行大量详细规划,每个人都在努力工作,尽可能快地推进这项试验。
安全性、不确定性、希望
总之,我们对首个针对亨廷顿病根本原因的药物人体试验最早将于明年开始感到兴奋。这种兴奋被以下认识所缓和:这第一个试验完全关注安全性,只涉及极少数亨廷顿病患者,而且研究的许多细节仍不确定。
与ASO-Htt-Rx类似的药物已在亨廷顿病动物模型中安全地恢复了健康行为,将治疗推进到人体试验阶段对整个亨廷顿病群体来说都是令人兴奋的一步。我们将密切关注试验的进展,希望能够不时提供谨慎的乐观信息。


