抑制免疫系统有助于亨廷顿氏症小鼠
通过抑制免疫系统,CB2 激活药物改善亨廷顿氏症小鼠的存活率和症状
注意事项自动翻译 – 可能出错
为了尽快向尽可能多的人传播高清研究新闻和试验更新,本文由人工智能自动翻译,尚未经过人工编辑审核。虽然我们努力提供准确、易懂的信息,但人工智能翻译可能会出现语法错误、误读或用词不清。如需获取最可靠的信息,请参阅英文原文,或稍后再查看经过人工编辑的译文。如果您发现重大问题,或者您的母语是英语,并希望帮助提高翻译的准确性,请随时通过 editors@hdbuzz.net 联系我们。
研究认为免疫系统在亨廷顿氏症中表现异常。现在,一种激活免疫细胞上 CB2 受体的药物已被证实可以改善 HD 小鼠的症状和存活率——这对于将免疫系统作为 HD 治疗靶点具有重要意义。
HD 中的免疫系统
亨廷顿氏症被称为神经退行性疾病,因为大多数症状是由神经元功能障碍和死亡引起的。但导致 HD 的突变型亨廷廷蛋白是由体内每个细胞产生的,近年来,研究人员已经开始在大脑之外寻找 HD 的治疗方法。
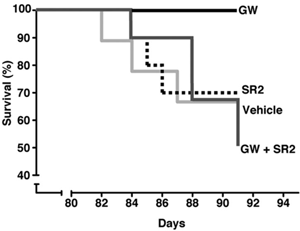
图片来源:神经科学学会(Bouchard 等人)
这种全身性研究方法的一个发现是,免疫系统——我们抵御感染和损伤的防御系统——在 HD 患者中似乎表现出轻微的差异。
平均而言,携带亨廷顿氏症突变的人体内被称为细胞因子的免疫信号分子水平高于正常水平,这种情况在症状出现之前就已存在。而且 HD 患者的白细胞反应过度——当它们在实验室中培养并用细菌产生的化学物质刺激时,它们产生的细胞因子比正常情况下更多。
HD 基因、免疫系统行为和大脑之间的联系仍在研究中。但已有迹象表明,人为改变免疫系统可能是对抗 HD 的一种方法。
去年,加利福尼亚格拉德斯通神经疾病研究所的 Paul Muchowski 博士带领的研究团队表明,使用一种名为 JM6 的药物改变白细胞的化学行为,可以延长亨廷顿氏症小鼠的寿命。今年早些时候,Muchowski 的团队报告称,将’正常’小鼠的骨髓移植到亨廷顿氏症小鼠体内具有轻微的益处。
因此,研究免疫系统以了解亨廷顿氏症,并将其作为可能的治疗靶点,目前是一个热门话题。在《神经科学杂志》发表的一篇新论文中,Muchowski 的团队再次取得突破——这次是一项关于免疫系统中’CB2 受体’活性的重要研究。
CB2 受体?
受体是从细胞表面伸出的分子,等待信号分子与之结合。当这种情况发生时,受体会触发细胞内一系列化学事件,最终改变细胞的行为。
每种受体只能’捕获’特定类型的信号分子,每种受体都会在细胞中引发一系列特定的事件。这就是我们体内每个细胞能够对各种信号做出适当反应的原理。
CB2 受体是’大麻素’受体家族的一部分。之所以这样命名,是因为它们可以被大麻中的化学物质激活。但是——需要明确的是,这不是一项关于大麻的研究!
CB2 受体的一个有趣特点是它们主要存在于免疫系统细胞上。激活 CB2 受体会’平静’这些免疫细胞,使它们产生较少的自身信号分子——即我们前面提到的细胞因子。
知道这一点,并且知道免疫系统在亨廷顿氏症中过度活跃,激活 CB2 受体应该是有益的。从另一个角度来看,禁用 CB2 受体在 HD 中可能是有害的。Muchowski 的团队研究了这两种可能性,从第二种开始。
敲除 CB2 基因
研究团队首先使用了一种名为BACHD的亨廷顿氏症模型动物,这种小鼠能产生人类突变型亨廷廷蛋白,并出现类似 HD 的症状。BACHD 小鼠的症状在大约六个月大时开始出现,并缓慢进展。
随后,他们使用基因工程技术制造了不含产生 CB2 受体基因的 BACHD 小鼠。以这种方式移除基因被称为基因’敲除’。
“当试验在十三周后停止时,30% 的未经治疗的小鼠已经死亡。但接受 GW 治疗的小鼠全部存活。”
没有 CB2 受体的 BACHD 小鼠比正常 BACHD 小鼠更早出现症状——在三个月而不是六个月时出现。
为了确认早期发病不仅仅是因为缺失 CB2 对大脑有害,Muchowski 的团队观察了第三组小鼠。这些小鼠缺乏 CB2 但不产生突变型亨廷廷蛋白。这些小鼠看起来很正常。只有当两种基因异常同时存在——产生突变型亨廷廷蛋白并且缺失 CB2——小鼠才会出现快速进展的症状。
而且这些小鼠不仅仅是症状更严重。研究人员检查了它们大脑中一种叫做
用药物激活 CB2:GW
CB2 敲除的结果表明 CB2 受体在抑制亨廷顿氏症症状方面发挥作用,Muchowski 的团队采取了下一步行动,试图增加 CB2 受体的活性。为此,他们使用了一种名为 GW405833 的CB2 激活药物,简称GW。
为了测试用 GW 激活 CB2 受体是否有帮助,研究人员使用了名为R6/2的亨廷顿氏症模型小鼠。这些小鼠在很年轻时就出现症状,并且病情发展迅速。
从四周龄开始,在症状刚出现后不久,就定期给 R6/2 小鼠注射 GW。通过测量它们的平衡能力来测试它们的运动症状。接受 GW 治疗的小鼠表现比未经治疗的小鼠更好——它们能在旋转杆上保持平衡的时间几乎是两倍。
R6/2 小鼠通常在大约五个月后死亡,但 GW 治疗产生了相当显著的效果。当试验在十三周后停止时,30% 的未经治疗的小鼠已经死亡。但接受 GW 治疗的小鼠没有一只死亡。当然,我们不知道它们在试验结束后还能活多久,但无论如何看,这都是令人震惊的结果。
之后,Muchowski 的团队测量了大脑中的突触素水平。回想一下,这些水平在 CB2 敲除小鼠中较低。在接受 GW 治疗的小鼠中,突触素水平较高,这表明 GW 的一个有益效果是改善神经元之间的连接。
在早期治疗取得如此好的结果后,研究人员重复了试验,将治疗开始时间推迟一个月到八周龄。那时,小鼠已经相当虚弱。但该药物对运动问题和大脑连接仍然有益。
血液还是大脑?
CB2 受体主要存在于免疫细胞上,而免疫细胞主要存在于血液、骨髓和脾脏中。大脑有自己的免疫细胞,称为小胶质细胞。因此,重要的是要问 GW 实际上在治疗哪些细胞。它是通过大脑中的小胶质细胞,还是通过体内的白细胞来改善症状?
Muchowski 的团队使用了一个巧妙的方法来找出答案。一些 R6/2 小鼠被给予两种药物。一种是 GW;另一种是一种名为 SR2 的 CB2’拮抗剂’。拮抗剂是一种阻断受体活性的药物。因此 SR2 和 GW 相互抵消,就如同没有给药一样。
这听起来并不特别巧妙,直到你了解到这些药物到达身体的不同部位。GW 可以到达所有地方——血液、器官和大脑。但 SR2不能到达大脑——它只停留在血液和器官中。因此,由于 SR2 在体内中和了 GW 的效果,同时使用两种药物治疗的小鼠只能在大脑中获得 GW 的效果。

如果 GW 在大脑中发挥作用,你会期望接受双重治疗的动物会改善——但它们没有。它们像未经治疗的小鼠一样生病和死亡。这表明 GW 的益处是通过其对大脑外免疫细胞的影响而产生的。
Muchowski 的另一种药物 JM6 也观察到类似的情况。总的来说,这些结果表明,改变体内免疫系统的行为可以对大脑产生有益影响,为对抗亨廷顿氏症开辟了许多新的攻击路线。
更进一步
GW 作用于免疫细胞如何使大脑受益?一种可能性是通过细胞因子的作用——我们前面提到的那些免疫信号分子。回想一下,亨廷顿氏症患者的血液样本中这些细胞因子的水平较高,特别是一种叫做 IL-6 的细胞因子。
当 Muchowski 的团队测量 GW 治疗组小鼠的 IL-6 水平时,他们发现水平降低了——实际上,GW 已经’平静’了过度活跃的免疫系统。因此这些勤奋的科学家进行了另一项药物试验来进一步研究 IL-6。
这次,他们给 R6/2 小鼠注射了一种抗体蛋白,这种抗体能够粘附在 IL-6 上并告诉身体将其清除。与未经治疗的小鼠相比,接受这种降低 IL-6 的抗体治疗的小鼠具有更好的运动控制能力。这种效果不如 GW 显著,但确实存在,这表明降低 IL-6 可能是 GW 的益处传递到大脑的一种方式。
总结
这项代表多年工作的研究给了我们很多思考的空间。
我们已经知道免疫系统在 HD 中表现出一些差异,但我们不太清楚直接治疗它是否是个好主意。
Muchowski 的研究提供了强有力的证据,表明 CB2 受体是体内免疫系统和大脑中亨廷顿氏症之间的重要联系。
GW 药物对这些病情严重的 R6/2 小鼠产生了相当显著的益处,但 GW 从未在人体中进行测试,因此需要进行大量的安全性测试以确保它不会造成伤害。一些国家已经批准了激活 CB 受体的药物(例如,用于多发性硬化症症状的 Sativex),但市场上还没有特定的 CB2 激活剂。
同样值得记住的是,其他在 R6/2 小鼠中显示改善的药物在人体试验中迄今尚未成功,因为没有任何动物能完美模拟亨廷顿氏症。
这项研究的一个有趣角度是 IL-6 抗体的轻微益处。有趣的是,这样的药物已经获准用于人类关节炎治疗——它叫做托珠单抗(或 Actemra)。在亨廷顿氏症中进行该药物的人体试验是可能的,而且可能比 GW 的试验更快开展。
最后——因为我们知道你们仍在想这个问题——这项研究不能告诉我们任何关于大麻是否对亨廷顿氏症患者有帮助的有用信息。虽然大麻确实含有激活 CB2 的分子,但它还含有数百种其他化学物质,其中许多具有其他生物学效应,这些都没有在 HD 中进行测试。因此,虽然我们知道大麻在 HD 及其他领域很受欢迎,但我们不能根据这项研究给予它科学认可。



