
强有力的信息:亨廷顿氏症中的有毒RNA信使分子是否会造成危害?
如果亨廷顿氏症的某些问题是由有害蛋白质以外的因素引起的呢?
研究人员长期以来认为亨廷顿氏症基因通过指导细胞产生有害蛋白质而导致问题。西班牙研究人员的一项引人入胜的新动物研究表明,我们可能需要关注多个可疑因素,才能完全解决亨廷顿氏症突变所引起的问题。
生物学的中心法则
每位亨廷顿氏症患者都携带相同的基本遗传突变,这种突变来自其父亲或母亲。为了简单起见,我们通常将这种突变基因称为HD基因。
导致亨廷顿氏症的突变是HD基因中已经重复的DNA片段的扩增。在基因的一端附近,我们发现遗传字母C-A-G反复重复。在没有亨廷顿氏症的人群中,他们的HD基因大约有20次这种CAG序列重复。然而,如果您继承了一个具有超过39次重复的HD基因副本,您将在生命中的某个时候发展出亨廷顿氏症。
细胞将基因用作指令或配方来创建蛋白质。蛋白质是使细胞运作的机器。我们细胞能够做的所有神奇的事情都依赖于在每个细胞内快速运转的数千种不同蛋白质的复杂相互作用。
在我们基因中的指令和在我们细胞中到处工作的蛋白质之间,存在一个中间步骤。由于DNA非常重要且必须不惜一切代价加以保护,当细胞需要特定蛋白质的副本时,细胞会将指令复制到一个新的分子中,这个分子被称为RNA。
因为它们在细胞的一个位置到另一个位置传递信息,科学家们将这些工作副本称为’信使RNA’或mRNA。
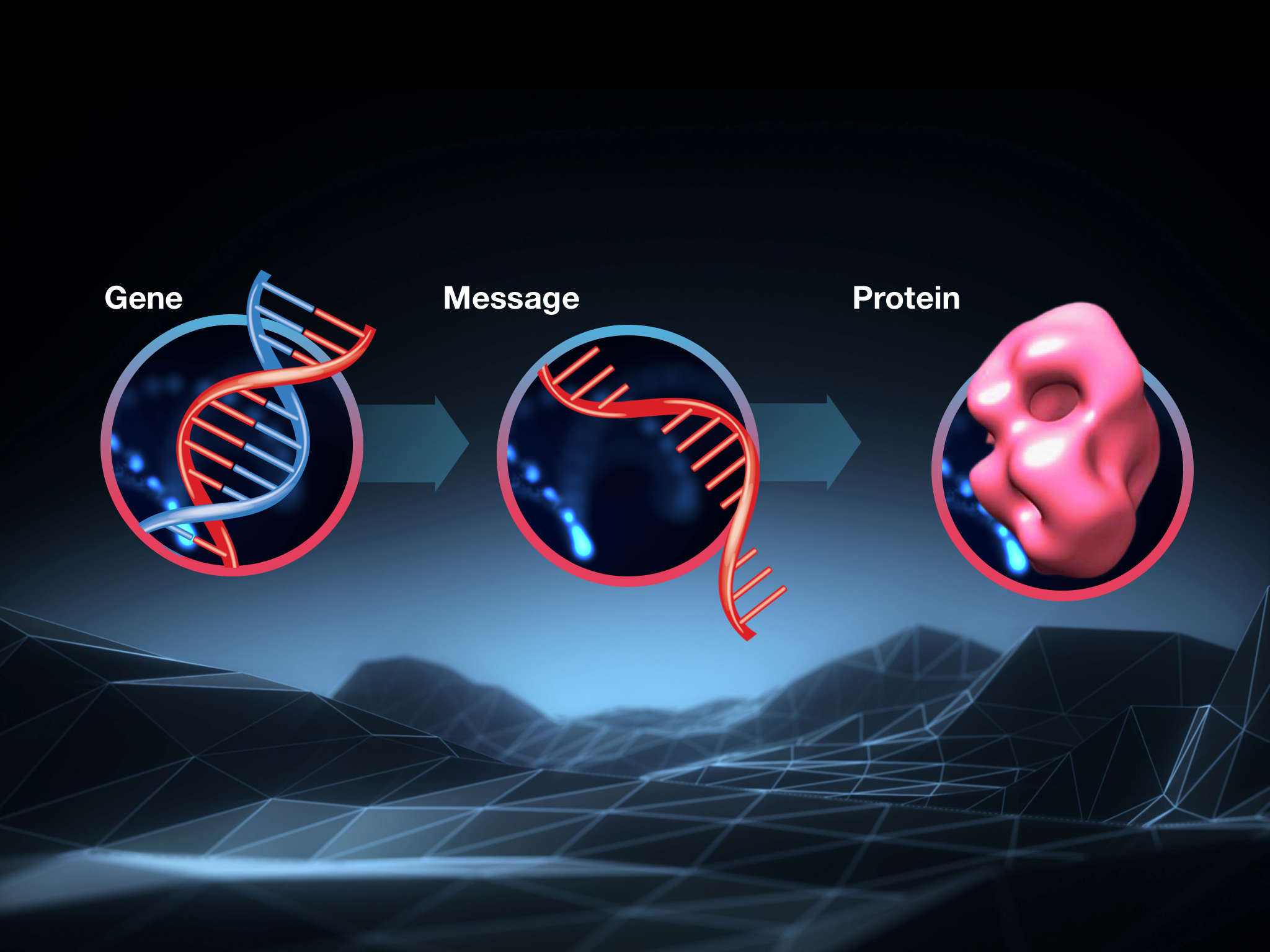
只要mRNA在周围漂浮,细胞就会读取它并遵循其指令来制造相应的蛋白质。这个序列 – 基因、mRNA、蛋白质 – 是所有细胞中实现和控制蛋白质制造的方式。它如此基础,以至于有时被称为’生物学的中心法则’。
谁是罪魁祸首?
这些参与者中谁是罪魁祸首?大多数研究亨廷顿氏症的科学家认为是突变蛋白质,而不是基因或信使,导致了携带亨廷顿氏症突变的人的细胞中的大多数问题。而且有大量证据表明蛋白质确实是导致携带HD突变的细胞出现许多问题的原因。但这就是全部真相吗?
在一些其他的遗传性疾病中,信使分子本身是导致问题的主要原因。一个例子是肌强直性营养不良,这种疾病也是由三个字母的遗传序列过度重复引起的。在肌强直性营养不良中,具有长重复序列的信息分子导致细胞工作不正常并最终死亡 – 是mRNA而不是相应的蛋白质造成了问题。
长期以来,一些科学家认为信使在亨廷顿氏症中也可能是有害的。来自西班牙一个研究小组的新工作表明,这些跳出框架思考的研究人员可能发现了一些重要线索。
细胞中的早期工作
2012年,由巴塞罗那大学的Eulalia Marti领导的一组研究人员描述了一些关于HD基因信使的非常有趣的工作。他们发现来自突变HD基因的信使分子 – 即在会发展成亨廷顿氏症的人群中发现的那种 – 对实验室中生长的细胞可能具有毒性。来自正常基因的信使分子对细胞并无毒性。
这很令人惊讶,因为研究团队已经仔细确保他们研究的信使分子不能实际指导细胞产生突变蛋白质。他们还进行了一些详细的后续实验,并确定了导致信使具有毒性的细胞中的一些关键参与者。
但是,仅仅因为某事可能在培养皿中的细胞中发生,并不意味着它确实在活体大脑中发生,所以Marti的团队接下来将注意力转向了亨廷顿氏症的小鼠模型和实际HD患者的大脑。在小鼠和人类的病变大脑区域中,他们发现了HD基因信使分子的有毒片段的证据。当他们仔细地从这些真实的大脑中清除所有蛋白质和其他物质,只留下信使分子时,他们发现这些信使分子使实验室中的健康细胞变得病态。
这是相当好的证据,表明HD基因的信使分子正在发生一些有趣的事情,而且很可能HD中细胞生病的一些原因可能是由突变蛋白质以外的东西引起的。
“这项新研究巧妙地证明了信使可能有害,并且这种危害可能具有重要意义。”
小鼠中的新研究
最近,Marti的团队发表了一项非常有趣的后续研究,表明他们可能发现了一些重要的东西。这项新研究使用了一种巧妙的方法来证明信使可能是有害的,而且这种危害可能很重要。
Marti和她的团队想出了一种方法来阻止HD基因信使分子的毒性,而不改变由HD基因产生的蛋白质水平。换句话说,信使仍然存在,并且仍然可以被蛋白质制造机器读取,但它不再能够直接造成危害。
令人惊讶的是,他们找到了一种方法来实现这一点,使用了所谓的反义寡核苷酸,即ASO。
如果您已经熟悉ASO,可能是因为它们目前正在亨廷顿氏症患者中进行测试,作为一种潜在的治疗方法。总的来说,ASO的工作是找到进入细胞的方式并粘附到信使分子上。
目前在人类中测试的ASO,由Ionis制药公司制造,能够粘附到HD基因信使分子上,并将其标记为待销毁目标。更少的信息意味着更少的蛋白质 – 我们希望这将保护细胞免受伤害。这种方法被称为亨廷廷降低或有时称为基因沉默。
但Marti和她的同事使用的ASO以一种微妙的不同方式工作。它们进入细胞并找到HD信使分子,但一旦找到它,它们就只是粘附在上面并停留在那里。不会破坏HD信使,因此也不会改变使用该信息的蛋白质水平。
为什么我们会想要这样一个看似无用的ASO?因为Marti的团队发现,通过与HD基因信息结合,他们在早期研究中发现的信息的毒性效应被阻断了。简而言之,他们找到了一个非常酷的工具来测试HD基因信使所扮演的角色的重要性。
当他们将这种特殊的ASO注射到HD模型小鼠的大脑中时,他们发现毒性信使效应减少了,但正如他们预测的那样,HD蛋白质没有变化。令人惊讶的是,他们发现尽管仍然存在大量的突变HD蛋白质,但小鼠的行为变得更健康了。
这一切意味着什么?
这是非常酷的科学,因为它做得非常仔细,并提醒我们必须继续质疑我们对HD如何工作的假设。像HD这样复杂的问题很可能有多个原因 – 突变基因产生的信使和蛋白质都可能具有毒性,这是完全合理的。
这对HD治疗,特别是正在进行的ASO亨廷廷降低试验意味着什么?我们还不确定,但直觉上,Ionis正在测试的ASO类型应该对两种类型的毒性效应都有益 – 无论是由信息还是由蛋白质引起的。许多其他亨廷廷降低方法也有望消除有毒的信使和蛋白质。即使某些未来的治疗’仅仅’降低蛋白质水平,我们仍然相当确信这将是一件非常好的事情。这真是令人欣慰!
现在Marti和她的团队已经指明了方向,研究人员将来可以检查任何新提出的治疗方法如何影响HD突变可能造成的两种类型的毒性。



