2016世界亨廷顿舞蹈症(HD)治疗学大会-第一天
蛋白质和DNA-Jeff和Ed从亨廷顿舞蹈症大会现场报告
 Professor Ed Wild撰写 2016年2月26日 Dr Jeff Carroll编辑 Xi Cao译制 最早发布于2016年2月24日
Professor Ed Wild撰写 2016年2月26日 Dr Jeff Carroll编辑 Xi Cao译制 最早发布于2016年2月24日
二月来了,世界顶尖的科学家们都在棕榈泉参加一年一度的亨廷顿舞蹈症大会。
周一晚-来自CHDI基金会的最新研究
在大会开始之前,CHDI的工作人员报告了可喜的科研进展。
汤姆.沃格特,CHDI基金会发现和系统生物的副总裁,同观众更新了CHDI基金会更好地理解亨廷顿舞蹈症的努力。沃格特提醒广大观众今年发布的一项大研究揭示了修正亨廷顿舞蹈症发病年龄的基因。这些基因可能有助于我们更好地了解亨廷顿舞蹈症的发生,但也为药物猎人提供重要的“目标”。为了实现这一突破,研究小组从上千位亨廷顿舞蹈症患者处获取了DNA样本。
另一项大研究,亨廷顿舞蹈症小鼠,已经产生了大量的关于亨廷顿舞蹈症突变影响不同组织的数据。更重要的是,这些新的数据集已经在网上可供世界各地的任何科学家使用。小鼠和人类的亨廷顿舞蹈症数据可以在这里找到它:https://www.hdinhd.org/

西莉亚-多明戈斯,CHDI基金会的化学部副总裁,在大会更新了基金会药物开发工作。研究亨廷顿舞蹈症患者和动物模型,是很重要的,但最终我们需要化学家来制造出可以提供给患者的药物。多明戈斯的团队不仅开发了实验性的药物,而且还开发了其他的新的化学物质,扩大了亨廷顿舞蹈症医师和科学家们的工作领域。
多明戈斯的团队正在寻找一种能降低突变亨廷顿舞蹈症蛋白水平的化学物质,这种蛋白是亨廷顿舞蹈症的诱因。CHDI基金会还在努力发展帮助细胞应对DNA损伤的药物,DNA损伤在亨廷顿舞蹈症中容易积累。来自小鼠的数据表明,调节细胞如何应对基因损伤,可以改善亨廷顿舞蹈症的症状。但是老鼠不是人,研究人员正在开发新的药物,希望能仿制小鼠身上的疗效。
最后,多明戈斯揭示了化学家们正在发展一种化学物质,可以让科学家看到亨廷顿舞蹈症患者的大脑。有一种化学标签,可以让科学家们测量活体病人大脑中有害亨廷顿舞蹈症蛋白的水平!多明戈斯的研究小组正在使用动物和人体组织的研究来探索这个新的化学物质是否和预期的一样有用。早期的研究看起来非常有前途,现在正迅速发展到人类的早期试验中。
如果这对人类有效,基因沉默试验将有一个强大的新手段来展示试验效率
克里斯蒂娜-桑帕约教授对CHDI基金会的临床试验项目进行了详细更新,包括项目引进活动。CHDI热衷于设计有动力的研究–就是说,有足够的参与者回答他们的研究问题。CHDI也旨在发布所有人都可以获得的数据。
星期二上午-亨廷顿蛋白
2016 亨廷顿舞蹈症大会以集中于亨廷顿蛋白的讨论开始,亨廷顿蛋白来自于亨廷顿舞蹈症基因。Elena Cattaneo教授提醒大家,亨廷顿舞蹈症基因的历史久远,第一次出现在8亿年前!而只有人类有亨廷顿舞蹈症,我们可以在海胆和黏菌里找到亨廷顿舞蹈症基因。很难研究它,因为它比平均人类基因大10倍左右。
细胞利用基因作为配方来构建细胞中的蛋白质。所以我们有一个HD基因和HD蛋白。很可能导致HD的脑细胞损伤是蛋白质的坏影响,而不是基因本身。
“DNA的损伤必须修复,但是似乎在HD基因中,这种普通的程序出了错。 ”
今天上午的会议重点是更好地了解这一重要的、古老的大蛋白质。更好地了解导致亨廷顿舞蹈症的蛋白质,有助于我们设计更好治疗方法。
来自USC的拉尔夫-兰根,采用一系列先进的成像技术来拍摄HD蛋白。兰根的团对研究HD蛋白的纯化部分,可以利用先进的工具推断它是如何成型的。在细胞中的蛋白质根据它们独特的形状进行分工。所以兰根的工作对理解HD蛋白工作至关重要。而且,也许最重要的是,兰根试图了解HD基因突变如何改变HD蛋白的结构。关于HD蛋白的有趣的一点是,当它发生突变后,它在细胞内开始结成块。一些科学家认为,这些团块,而不是单个的HD蛋白,导致脑细胞的问题。在兰根的实验室的另一项工作是了解当HD蛋白结块时,单个HD蛋白的结构如何改变。
Hilal Lashue是另一个研究HD蛋白形状的科学家。特别的是,Lashuel对HD蛋白的形状对“翻译后修饰”的反应感兴趣(!)蛋白质在细胞中被制成后,被不同的化学标签修饰,来改变蛋白质的形状。因此,对于蛋白质,形状决定功能,这些小标签调节蛋白质在细胞中的作用。为什么我们关心HD蛋白的化学标签?我们从小鼠研究知道,特定的标签减少HD蛋白的毒性。Lashuel的团队已经开发了合成大量特定的化学标签的HD蛋白的化学技术。这使得研究人员能够研究所有标签和功能的组合的影响。
长期研究HD的研究员Scott Zeitlin也试图了解HD变异蛋白。不通过试管和化学,Scott Zeitlin使用删减了HD基因的一小部分的小鼠。最简单的方法来研究,打破它,看看发生了什么!令人惊讶的是,Zeitlin发现他可以删除HD基因的重要区域却没有对小鼠产生重大影响。他是现在试图理解如果删除HD基因的重要部分,是否会使小鼠的HD样症状恶化
来自INSERM的Fred Saudou谈论了他关于HD蛋白在细胞中的作用的研究。主要的理论是,突变会导致该蛋白增加对神经元有害的的行为或功能。他说,HD蛋白有像弹簧一样的地区,这些地区看起来像几个小贼串在一起。众所周知的HD蛋白协助化学物质在我们的神经元周围移动。 亨廷顿蛋白协助于传送一个有益的被称为BDNF的化学物质从表面到大脑深部结构。我们需要BDNF来保持纹状体的细胞健康,而在HD中,BDNF降低和纹状体中的细胞死亡。Saudou说:HD中BDNF的传送失败可能是由于突变蛋白不能为细胞的分子马达提供能量。他从一种病毒中借来蛋白剪切酶,看看当切割HD蛋白的不同部位时,会发生什么?令人惊讶的是,他发现两个切割会使突变的HD蛋白产生毒性。
这很有趣-我们以前认为细胞剪切酶在正确的地方的一次切割,就足够产生毒性了。Saudou发现蛋白质的C末端比他以前认为的更重要。似乎某些片段的C-末端本身是有毒的,即便是蛋白没有毒性的时候。有趣!但是非突变蛋白并不是有毒的,因此在C-末端和突变改变的部分肯定有相互作用。Saudou发现HD蛋白C-末端点干扰另一种称为动力1的蛋白质,这种蛋白质对运输很重要。
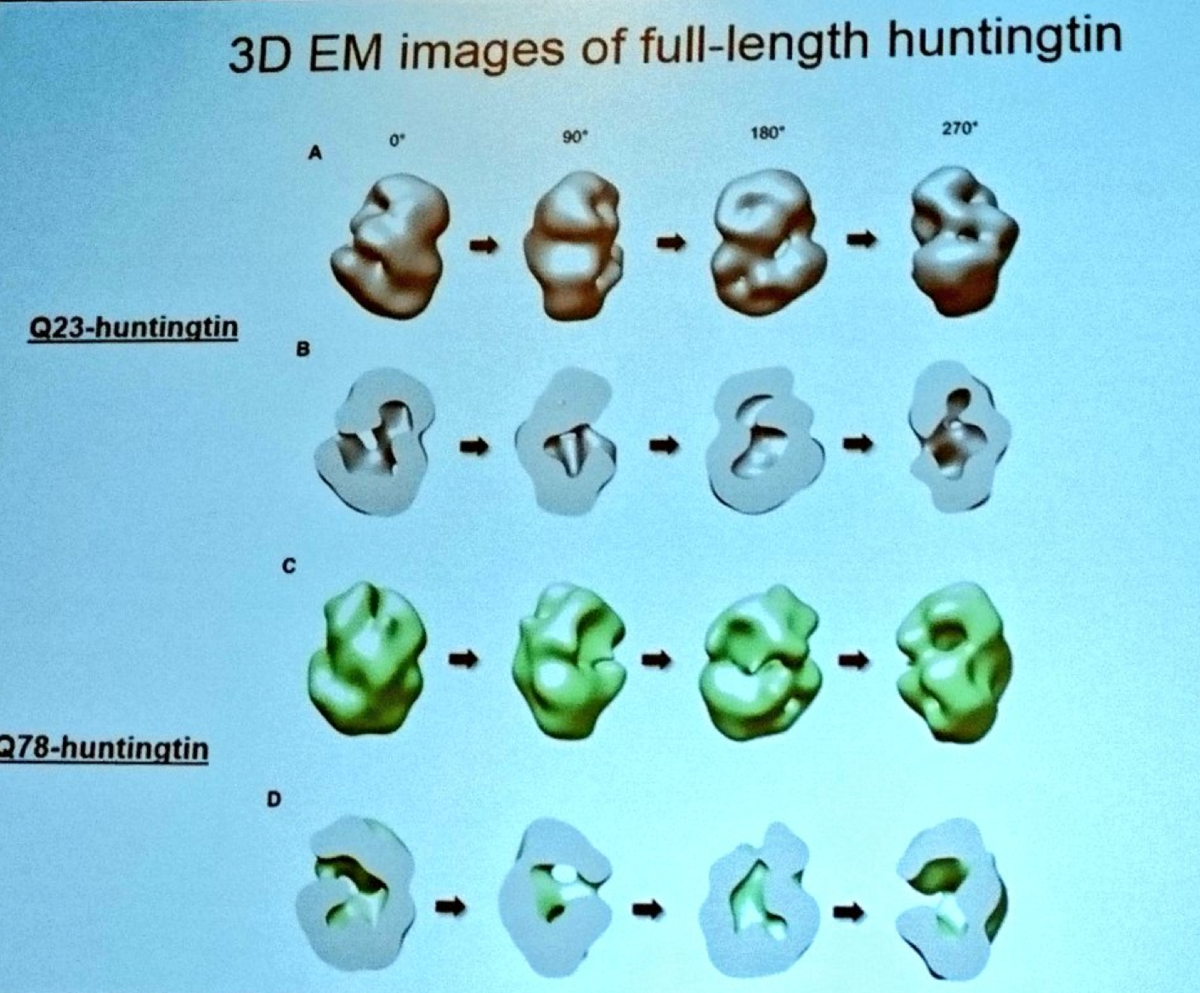
接下来我们听到了来自马萨诸塞州总医院的Ihn Sik Seong的研究。Sik Seong已发展出净化整个HD蛋白来研究其结构的技术。使用超级强大的电子显微镜,他开发了亨廷顿蛋白的一个外观模型。因为他可以制造正常和突变的HD蛋白,能看到蛋白质的整体形状是如何被突变改变。该模型表明,亨廷顿蛋白会自己折叠,形成一个像网球一样的中空的形状。他正在努力了解化学标记如何修改HD蛋白。
所有这一切研究HD突变对HD蛋白影响的基础科学将促进研究新发现的下一个浪潮!
星期二下午-DNA和RNA
今天下午我们将继续以基本科学为主题,谈论DNA。敬请关注! 来自UCLA的Steve Horvath对DNA衰老中的化学变化感兴趣。其中的一个化学变化有很强的可复制性,Horvath可以用它作为时钟来预测一个细胞的年龄。使用这种基因时钟,Horvath发现身体的不同部位以不同的速率“老化”。那么像HD这种脑部疾病患者的大脑样本有什么发现呢?HD患者的脑部比正常人快吗?是的。 Horvath发现HD的大脑看起来比较老化。
Karine Merienne在研究一个称为“转录”的过程,即在HD中细胞决定需要制造哪些基因的过程。人类身体的每一个细胞都有一个大约25000个遗传自父母的基因复制。脑细胞需要脑基因,皮肤细胞需要皮肤基因。“转录”是开启正确的基因的过程。激活基因模式在HD患者的大脑中被改变,她在使用HD小鼠试图理解为什么会这样。她发现一个特定的过程似乎在HD细胞中出错,这可能有助于解释一些转录过程的变化。一种实验性的药物改善这一特定的转录过程,似乎能保护HD小鼠的记忆功能。
凡妮莎-惠勒在研究在老化过程中,导致HD的变异如何在特定组织中恶化。每个HD患者都遗传了其DNA中的一个特定变化,HD基因中CAG序列的膨胀。在HD患者中,CAG重复序列总是长于正常,重复36次以上。一般来说,一个较长的CAG重复导致早年病发,虽然因人而异。惠勒的实验室对一个奇怪的现象感兴趣,在身体的某些组织里,随着年龄的增长,CAG重复序列越长。纹状体-大脑中受HD影响最大的部分,是发生CAG扩张最频繁的身体部位。
惠勒想弄明白为什么在身体的某些部位,CAG重复长度有随年龄增加的趋势。惠勒的团队发现,一个称为DNA修复的过程导致HD基因中CAG重复区域的扩大。DNA的损伤必须修复,但似乎这种正常的程序在此处出错。最近的HD患者一项研究表明,人们对DNA损伤的不同反应可能有助于解释发病年龄的变化。惠勒在进行广泛的新小鼠试验,更好的了解这个“CAG扩张”过程中发生的事情。 接下来自佛罗里达大学的 Laura Ranum谈论了一个新的且有争议的观点。想一想这个词CART。如果你读最开始的三个字母,是英文里的汽车。但是如果你从第二个字母开始,是英文艺术。当细胞阅读时DNA信息时,类似的事情会发生。大多数的时候,阅读从开头开始,但偶尔读取的顺序会被打乱,产生RNA信息或甚至是意想不到的蛋白质。偶尔DNA甚至向后读取产生奇怪的“隐藏”的RNA信息或蛋白质。她发现了这个奇怪的DNA阅读机制,称之为RAN译。
在HD,我们知道在正常的阅读方式产生突变HD蛋白,我们知道它对神经元有害。问题是,突变的HD蛋白是否扩张基因的唯一有毒的产品,是扩大基因只有毒的产品,或者RAN译是否导致有毒的RNA或者其他蛋白。Ranum的团队从死去的HD患者的脑组织样本发现了在一些地区的奇怪蛋白质。在大脑中发现这些蛋白质是一个开始,但并不意味着它们会造成伤害。在实验室培养的细胞中,她已发现出一些RAN蛋白可能是有害的——尽管这并不一定转送到整个大脑。
Ray Truant (麦克马斯特大学)想了解HD蛋白都干些什么,以及突变如何导致HD基因改变它的日常职能。像许多今天的演讲者一样,他对装饰HD蛋白的小化学标签特别感兴趣。他使用机器人显微镜和先进的软件自动分析药物对HD细胞的影响。使用这些技术,他的实验室跟踪暴露于各种不同应激环境中的细胞的HD蛋白。发现一种称为激动素的化学物质有助于保持突变HD细胞健康。
当给HD小鼠使用激动素,一些HD样症状有改善,支持了这种分子可能会有所帮助的想法。他的实验室也做了大量的实验表明,HD蛋白可能参与了DNA损伤。他的假设是,激动素有助于突变的HD蛋白更好地应对DNA损伤。他暗示HD蛋白可能在DNA损伤中起一定作用,提出研究激动素作为一个潜在的HD治疗方法。


